アメリカ食品医薬品局が突如モデルナのmRNAインフルエンザワクチンの承認を拒否しその後撤回
mRNAワクチンのパイオニアであるモデルナがmRNAインフルエンザワクチンの審査を医薬品の規制を担当するアメリカ食品医薬品局(FDA)に申請したところ、これを拒否されるという事態が起きました。しかし、FDAはこの拒否を撤回しています。
Moderna Announces the U.S. Food and Drug Administration will Initiate the Review of Its Investigational Seasonal Influenza Vaccine Submission
https://feeds.issuerdirect.com/news-release.html?newsid=8923338804483797

FDA reverses surprise rejection of Moderna's mRNA flu vaccine - Ars Technica
https://arstechnica.com/health/2026/02/fda-does-u-turn-will-review-modernas-mrna-flu-shot-after-shocking-rejection/
現地時間の2026年2月11日、モデルナは季節性インフルエンザワクチン「mRNA-1010」の治験のために生物学的製剤承認申請をFDAに行なったところ、これを拒否されたことを明かしました。FDAはモデルナの第3相試験の設計が審査拒否の理由と説明していますが、mRNA-1010はすでにEU、カナダ、オーストラリアで同様の申請を受理されており、申請前に行なわれた協議でのフィードバックと矛盾しているとして、審査拒否は予想外の出来事であったことを明かしています。
Moderna Receives Refusal-to-File Letter from the U.S. Food and Drug Administration for Its Investigational Seasonal Influenza Vaccine, mRNA-1010
https://feeds.issuerdirect.com/news-release.html?newsid=7346090610333866

モデルナの第3相試験では、mRNA-1010の安全性と有効性を検証するために約4万1000人の参加者が、グラクソ・スミスクラインの季節性インフルエンザワクチンであるフルアリックスを含む、FDAの承認を受けた標準用量のインフルエンザワクチンを対照ワクチンとして利用しています。その結果、対照ワクチンと比べてmRNA-1010は26.6%高い有効性を確認されたことが、2025年7月に報告されていました。
mRNAインフルエンザワクチンの効果が従来のワクチンを上回ったとモデルナが発表 - GIGAZINE
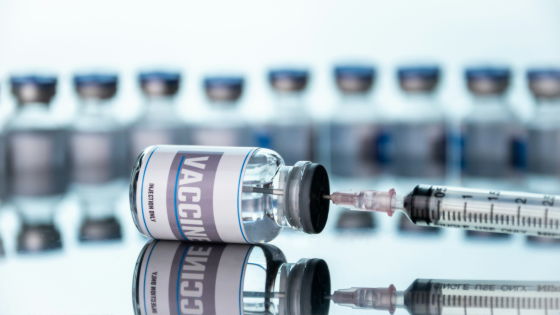
モデルナによると、FDAはmRNA-1010の生物学的製剤承認申請前に、少なくとも2024年4月と2025年8月の2回にわたって試験設計を審査・承認しています。
モデルナのステファン・バンセルCEOは、「FDAの生物製剤評価研究センター(CBER)による今回の決定は、モデルナ製品の安全性や有効性に関する懸念を一切特定しておらず、革新的医薬品開発におけるアメリカのリーダーシップを強化するという我々共通の目標達成に寄与するものでもありません」「FDAが承認ワクチンを比較対照としたインフルエンザワクチン申請について、CBERと事前に協議し合意した試験において、包括的な審査を行うことに議論の余地がないはずです」とFDAによる審査拒否に疑問を呈しています。
FDAによるモデルナのmRNA-1010の審査拒否判断は、トランプ政権においてワクチン規制当局のトップを務めるヴィナイ・プラサド氏が下したものです。Stat Newsの報道により、この判断はFDAの科学者の意見を却下し、プラサド氏が単独で下した決定であることが明らかになっています。実際、FDAでワクチン審査を担当する上級官僚のデビッド・カスロー氏によると、FDAの科学者チームがmRNA-1010の審査準備を整えており、審査を進めるべき状況にあることをプラサド氏に説明しています。カスロー氏も審査を進めるべき理由をまとめたメモをプラサド氏に提出したそうですが、これらを無視してプラサド氏は審査を拒否したわけです。
プラサド氏は審査拒否の理由として、mRNA-1010が第3相試験で対照ワクチンとして使用したフルアリックスを挙げており、「利用可能な最善の標準的な治療を反映していない」ため、臨床試験は「適切に管理されたもの」ではなかったと指摘していました。
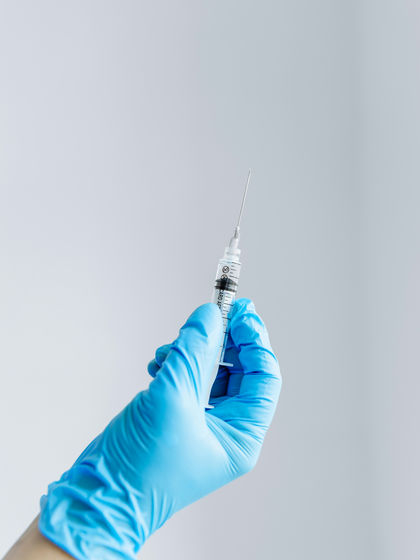
しかし、現地時間の2026年2月18日、モデルナはFDAがmRNA-1010の生物学的製剤承認申請の審査を進めると通知してきたことを明かしました。モデルナはFDAの審査拒否に対して協議を行い、審査拒否の見直しに同意してもらうことができたと説明しています。
バンセルCEOは「FDAの承認を待ち、2026年後半にはmRNA-1010の提供を開始し、アメリカの高齢者がインフルエンザから身を守るための新しい選択肢を提供できるようになることを期待しています」と語りました。なお、FDAは2026年8月5日までにワクチンの承認に関する決定を下す見込みです。
アメリカ合衆国保健福祉省の広報担当者であるアンドリュー・ニクソン氏はArs Technicaに対して、「モデルナとの協議の結果、規制上のアプローチの見直しと申請の修正が行われ、FDAはこれを受理しました。FDAは他のすべての製品と同様に、審査および認可の段階においても高い基準を維持していきます」と述べ、審査拒否を撤回したことを明かしています。
・関連記事
新型コロナのmRNAワクチンは「がんと戦う免疫システム」を活性化する可能性 - GIGAZINE
mRNAインフルエンザワクチンの効果が従来のワクチンを上回ったとモデルナが発表 - GIGAZINE
モデルナのmRNAがんワクチンと抗体医薬品「キイトルーダ」の併用で悪性黒色腫の再発・死亡リスクが半減 - GIGAZINE
モデルナが結核やマラリアなど「最も危険とされる感染症15種」に対するmRNAワクチンの開発計画を発表 - GIGAZINE
新型コロナのワクチンに用いられる「mRNA」とは何なのか、何ができて何ができないのか? - GIGAZINE
・関連コンテンツ
in サイエンス, Posted by logu_ii
You can read the machine translated English article US Food and Drug Administration suddenly….