タンパク質の立体構造を正確に予測するAI「AlphaFold」の最新版がリリース、従来よりも高精度な分子の予測が可能に
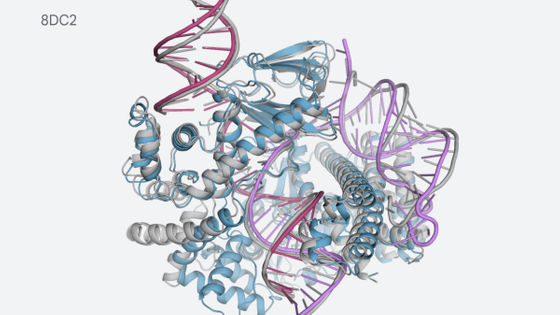
Googleの人工知能関連企業であるGoogle DeepMindは、2018年にアミノ酸の塩基配列情報からタンパク質の立体構造を予測できるAI「AlphaFold」を発表しました。AlphaFoldはその後も改良が重ねられ、2023年10月30日にリリースされたAlphaFoldの最新版では、従来よりも予測の精度が大幅に向上し、タンパク質だけでなく、リガンドなどの生体分子の予測も可能になったとのことです。
A glimpse of the next generation of AlphaFold - Google DeepMind
https://deepmind.google/discover/blog/a-glimpse-of-the-next-generation-of-alphafold/

DeepMind’s latest AlphaFold model is more useful for drug discovery | TechCrunch
https://techcrunch.com/2023/10/31/deepminds-latest-alphafold-model-is-more-useful-for-drug-discovery/
Google DeepMind boss hits back at Meta AI chief over ‘fearmongering’ claim
https://www.cnbc.com/2023/10/31/google-deepmind-boss-hits-back-at-meta-ai-chief-over-fearmongering-claim.html
Google Brain founder says big tech is lying about AI extinction danger
https://www.afr.com/technology/google-brain-founder-says-big-tech-is-lying-about-ai-human-extinction-danger-20231027-p5efnz
筋肉の収縮や血液の輸送、光の感知、食物のエネルギー変換など、あらゆる生物学的プロセスに関連するタンパク質は、20種類ものL-アミノ酸が鎖状に連結した立体的な高分子化合物です。これまでに人間が発見したタンパク質の種類は2億を超えていますが、立体構造が特定されているタンパク質は少数です。
しかし、Google DeepMindが開発したAlphaFoldは、これまで立体構造が不明だったタンパク質の構造をAIを用いて予測しており、2020年にはAlphaFoldが従来の低温電子顕微鏡法などの実験的手法によるタンパク質の立体構造の解析が同レベルの精度を記録したことが報告されています。
AlphaFoldには「タンパク質のフォールディング問題」と呼ばれる、長年にわたり生物学上の大きな問題となっている、アミノ酸配列からの立体構造の予測が困難という問題を解決できる可能性について、期待が寄せられています。
タンパク質の立体構造を予測するAI「AlphaFold」はどのように生物学の世界を変えているのか? - GIGAZINE

これまでGoogle DeepMindは、2020年に従来のAlphaFoldの改良版であるAlphaFold2をリリースしたり、2021年にはAlphaFoldをオープンソース化したり
そして、2023年10月31日にリリースされたAlphaFoldの最新版では、世界最大の生体分子のオープンアクセスデータベースである「タンパク質構造データバンク」に網羅されたほぼ全ての分子の立体構造を予測できることが報告されています。
Excited to share major progress on next generation of AlphaFold! Together with @IsomorphicLabs, we’ve significantly advanced accuracy & expanded coverage beyond proteins to other key biomolecular classes. Continuing to accelerate science at digital speed https://t.co/zmR06BlrQx
— Demis Hassabis (@demishassabis) October 31, 2023
また、Google DeepMindによると、新たなAlphaFoldでは、生体分子と複合体を形成して生物学的な目的を果たす「リガンド」と呼ばれる物質や、タンパク質が作られた後に起こる化学変化に伴う分子構造も正確に予測できるとのこと。
これまで、製薬研究者は「ドッキング法」と呼ばれるコンピューターシミュレーションを用いて、タンパク質とリガンドがどのように相互作用するかについて検討を行っていました。しかし、ドッキング法ではタンパク質の構造などが重要となり、ドッキング法を用いた製薬技術には限界がありました。新たなAlphaFoldでは、タンパク質の構造などはAIが自動で予測するため、これまで立体構造が明らかにされていなかったタンパク質の予測を行うと同時に、タンパク質や核酸が他の分子とどのように相互作用するかについて詳細なシミュレーションを行うことが可能です。
Google DeepMindが公開したAlphaFoldのデモ映像が以下。
Series of predicted structures compared to ground truth (white) from our latest AlphaFold model. - YouTube
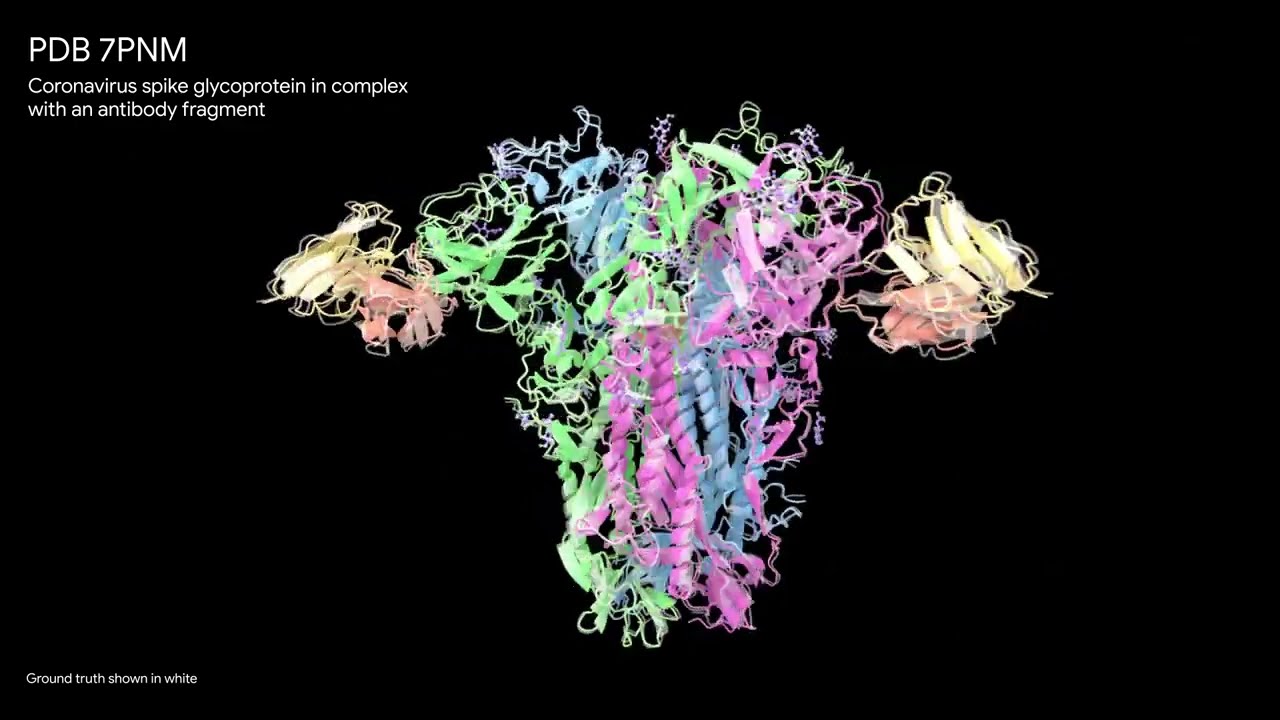
Google DeepMindは「抗体の結合など、創薬に関連するさまざまなタンパク質構造の予測問題について、新たなAlphaFoldは従来のAlphaFoldの成績を大幅に上回っています。今回のAlphaFoldの劇的な性能向上は、人体を構成する分子の科学的理解が大幅に進む可能性があり、AIの有用性を示しています」と述べています。
一方で、Google DeepMindは体内のRNA分子構造を予測することについて、AlphaFoldが従来の方法に劣っていることを(PDFファイル)報告しており、解決に向けてさらなる研究を行っていることを明かしています。また、Google DeepMindの関連企業であるIsomorphic Labsは、すでに新たなAlphaFoldを治療薬の設計に導入しており、AlphaFoldが病気の治療に重要なさまざまな分子構造の解析に役立っていることを報告しています。
Google DeepMindのデミス・ハサビスCEOは「汎用(はんよう)人工知能」と呼ばれる、さまざまな分野で人間をしのぐ性能の人工知能が最終的に誕生するだろうと予測しており、AIの暴走や犯罪に用いられる危険性を危惧し、早急な人工知能の規制の導入を求めています。
一方でGoogleの人工知能開発チーム「Google Brain」の共同創設者であるアンドリュー・ウン氏は「人工知能が人間を絶滅させるという考え方は、AI市場での競争を避けるための規制の導入を期待した大手AI関連企業による『悪い考え』です」「この考えはAIに関する新たなイノベーションをつぶしてしまう可能性があります」と指摘しています。
・関連記事
タンパク質の立体構造を予測するAI「AlphaFold」はどのように生物学の世界を変えているのか? - GIGAZINE
人工知能企業DeepMindがタンパク質構造解析アルゴリズム「AlphaFold」をオープンソースで公開、誰でも利用可能に - GIGAZINE
タンパク質の立体構造を予測するシステムが機械学習によって大きく進歩している - GIGAZINE
50年前からの生物学の超難問にDeepMindの開発した「AlphaFold」がAIのパワーで道筋を示し研究が加速 - GIGAZINE
Google DeepMindがAI「AlphaMissense」を発表、どの遺伝子変異が有害かを予測して遺伝性疾患の原因を特定するのに役立つ可能性 - GIGAZINE
・関連コンテンツ
in 動画, ソフトウェア, サイエンス, Posted by darkhorse_log
You can read the machine translated English article The latest version of the AI 'AlphaFold'….